《2022年高考化學(xué)復(fù)習(xí) 拓展精練選擇題(47)》由會(huì)員分享����,可在線(xiàn)閱讀�����,更多相關(guān)《2022年高考化學(xué)復(fù)習(xí) 拓展精練選擇題(47)(2頁(yè)珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索��。
1�、2022年高考化學(xué)復(fù)習(xí) 拓展精練選擇題(47)
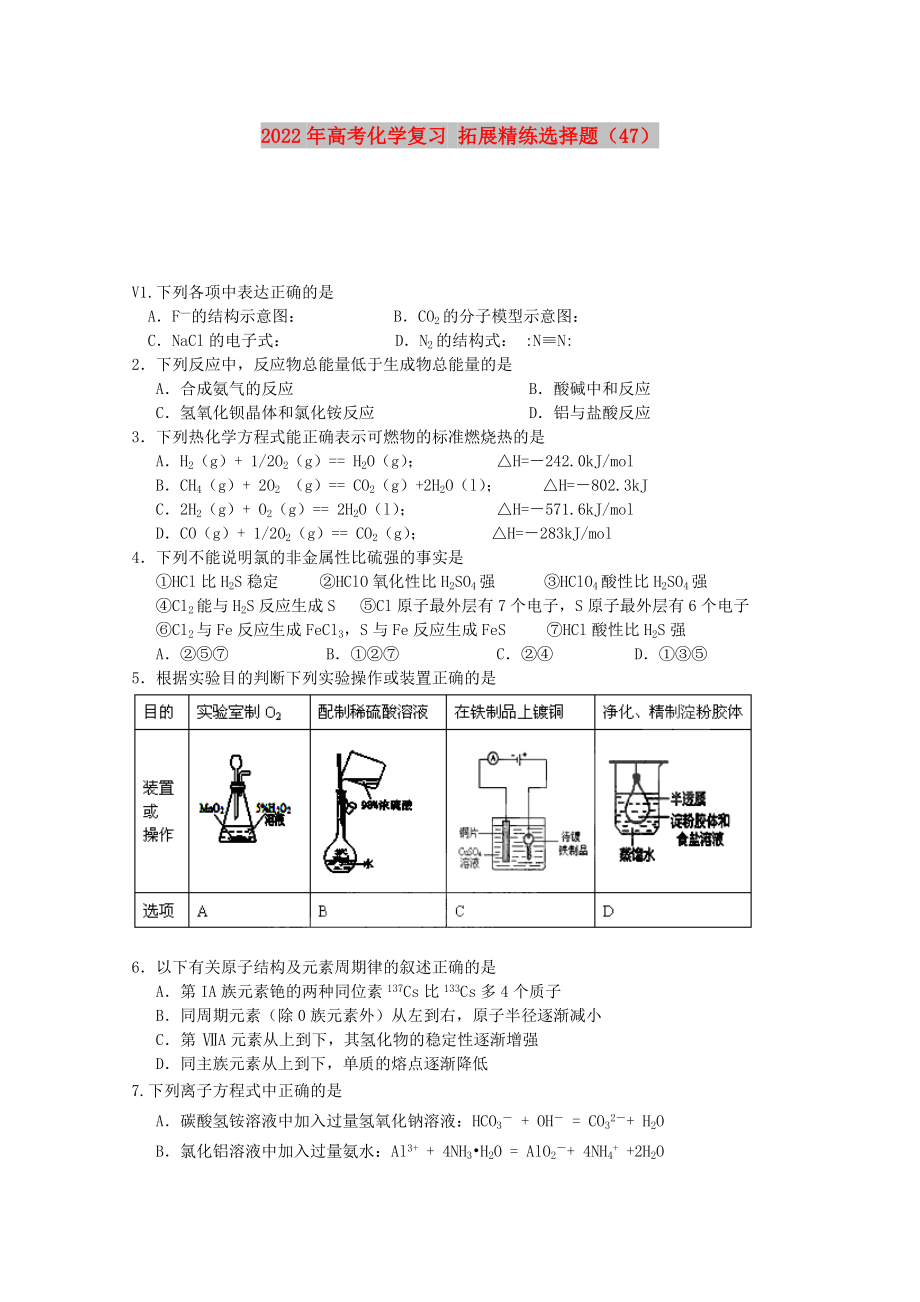
V1.下列各項(xiàng)中表達(dá)正確的是
A.F—的結(jié)構(gòu)示意圖: B.CO2的分子模型示意圖:
C.NaCl的電子式: D.N2的結(jié)構(gòu)式: :N≡N:
2.下列反應(yīng)中,反應(yīng)物總能量低于生成物總能量的是
A.合成氨氣的反應(yīng) B.酸堿中和反應(yīng)
C.氫氧化鋇晶體和氯化銨反應(yīng) D.鋁與鹽酸反應(yīng)
3.下列熱化學(xué)方程式能正確表示可燃物的標(biāo)準(zhǔn)燃燒熱的是
A.H2(g)+ 1/2O2(g)
2����、== H2O(g); △H=-242.0kJ/mol
B.CH4(g)+ 2O2 (g)== CO2(g)+2H2O(l)�; △H=-802.3kJ
C.2H2(g)+ O2(g)== 2H2O(l); △H=-571.6kJ/mol
D.CO(g)+ 1/2O2(g)== CO2(g)��; △H=-283kJ/mol
4.下列不能說(shuō)明氯的非金屬性比硫強(qiáng)的事實(shí)是
①HCl比H2S穩(wěn)定 ②HClO氧化性比H2SO4強(qiáng) ③HClO4酸性比H2SO4強(qiáng)
④Cl2能與H2S反應(yīng)生成S ⑤Cl原子最外層有
3�、7個(gè)電子,S原子最外層有6個(gè)電子
⑥Cl2與Fe反應(yīng)生成FeCl3����,S與Fe反應(yīng)生成FeS ⑦HCl酸性比H2S強(qiáng)
A.②⑤⑦ B.①②⑦ C.②④ D.①③⑤
5.根據(jù)實(shí)驗(yàn)?zāi)康呐袛嘞铝袑?shí)驗(yàn)操作或裝置正確的是
6.以下有關(guān)原子結(jié)構(gòu)及元素周期律的敘述正確的是
A.第IA族元素銫的兩種同位素137Cs比133Cs多4個(gè)質(zhì)子
B.同周期元素(除0族元素外)從左到右,原子半徑逐漸減小
C.第 ⅦA元素從上到下,其氫化物的穩(wěn)定性逐漸增強(qiáng)
D.同主族元素從上到下��,單質(zhì)的熔點(diǎn)逐漸降低
7.下列離子方程式中正
4�����、確的是
A.碳酸氫銨溶液中加入過(guò)量氫氧化鈉溶液:HCO3- + OH- = CO32-+ H2O
B.氯化鋁溶液中加入過(guò)量氨水:Al3+ + 4NH3?H2O = AlO2-+ 4NH4+ +2H2O
C.二氧化氮通入水中:3NO2 + H2O = 2H+ + 2NO3— + NO
D.氯氣通入水中的反應(yīng):Cl2+H2O = 2H++ Cl— + ClO—
8.右圖是一原電池的裝置����,關(guān)于它的說(shuō)法正確的是
A.裝置中銅是負(fù)極
B.銅表面的反應(yīng)為:2H++2e-=H2↑
C.電流的方向是從鐵經(jīng)導(dǎo)線(xiàn)流向銅
D.構(gòu)成原電池后����,鐵與硫酸銅的反應(yīng)速率加快
9.已知短
5、周期元素的離子: aA2+����、bB+、cC3-�����、dD-都具有相同的電子層結(jié)構(gòu)��,則下列敘述正確的是
A.原子半徑 A>B>D>C B.原子序數(shù)d>c>b>a
C.離子半徑 C>D>B>A D.單質(zhì)的還原性 A>B>D>C
10.元素的原子結(jié)構(gòu)決定其性質(zhì)和在周期表中的位置�����。下列說(shuō)法正確的是
A.元素原子的最外層電子數(shù)等于元素的最高化合價(jià)
B.多電子原子中,在離核較近的區(qū)域內(nèi)運(yùn)動(dòng)的電子能量較高
C.P���、S�、Cl得電子能力和最高價(jià)氧化物對(duì)應(yīng)的水化物的酸性均依次增強(qiáng)
D.元素周期表中位于金屬和非金屬分界線(xiàn)附近的元素屬于過(guò)渡元素
11.
6�����、下列實(shí)驗(yàn)過(guò)程中��,始終無(wú)明顯現(xiàn)象的是
A.NO2通入FeSO4溶液中 B. NH3通入AlCl3溶液中
C.CO2通入CaCl2溶液中 D.SO2通入已酸化的Ba(NO3)2溶液中
12.下列各組離子在指定溶液中能大量共存的是
①無(wú)色溶液中:K+����、Na+、Cu2+�、OH-
②pH=11的溶液中:CO32-、Na+���、AlO2-��、NO3-
③加入Al能放出H2的溶液中:Cl-����、HCO3-、SO42-�、NH4+
④由水電離出的c(OH-)=10-13mol·L-1的溶液中:Na+、Ba2+����、Cl-、Br-
⑤有較多Fe3+的溶液中: Na+�、NH4+、SCN-���、HCO3-
⑥酸性溶液中:Fe2+��、Al3+�����、NO3-、I-�、Cl-
A.①② B.③⑥ C.②④ D.③⑤
參考答案
A
C
D
A
D
B
C
D
C
C
C
C
 2022年高考化學(xué)復(fù)習(xí) 拓展精練選擇題(47)
2022年高考化學(xué)復(fù)習(xí) 拓展精練選擇題(47)