《天津市太平村中學(xué)2020年中考化學(xué)考點(diǎn)訓(xùn)練 質(zhì)量守恒定律(無(wú)答案)》由會(huì)員分享���,可在線(xiàn)閱讀�����,更多相關(guān)《天津市太平村中學(xué)2020年中考化學(xué)考點(diǎn)訓(xùn)練 質(zhì)量守恒定律(無(wú)答案)(2頁(yè)珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索。
1����、考點(diǎn)10 質(zhì)量守恒定律
選擇題
1、 我市某縣一副長(zhǎng)酒后駕車(chē)將受到法律追究�����。交警常用一種“酒精檢測(cè)儀”檢查司機(jī)是否酒后駕車(chē)�����。其反應(yīng)原理為C2H5OH + 4CrO3 + 6H2SO4 = 2X + 2CO2↑+9H2O,反應(yīng)中紅色的CrO3轉(zhuǎn)化為綠色的化合物X�����,則X的化學(xué)式為( )
A、Cr2O3 B����、CrSO3 C、Cr2(SO4)3 D�、Cr2S3
2、 為防止硝酸廠(chǎng)產(chǎn)生的氮氧化物污染環(huán)境�,通常用NaOH溶液吸收這些氮氧化物,反應(yīng)的化學(xué)方程式為:NO+NOx+2NaOH=2NaNO2+H2O���,方程式中x的值是
2���、( )
A.1 B.2 C.3 D.任意值
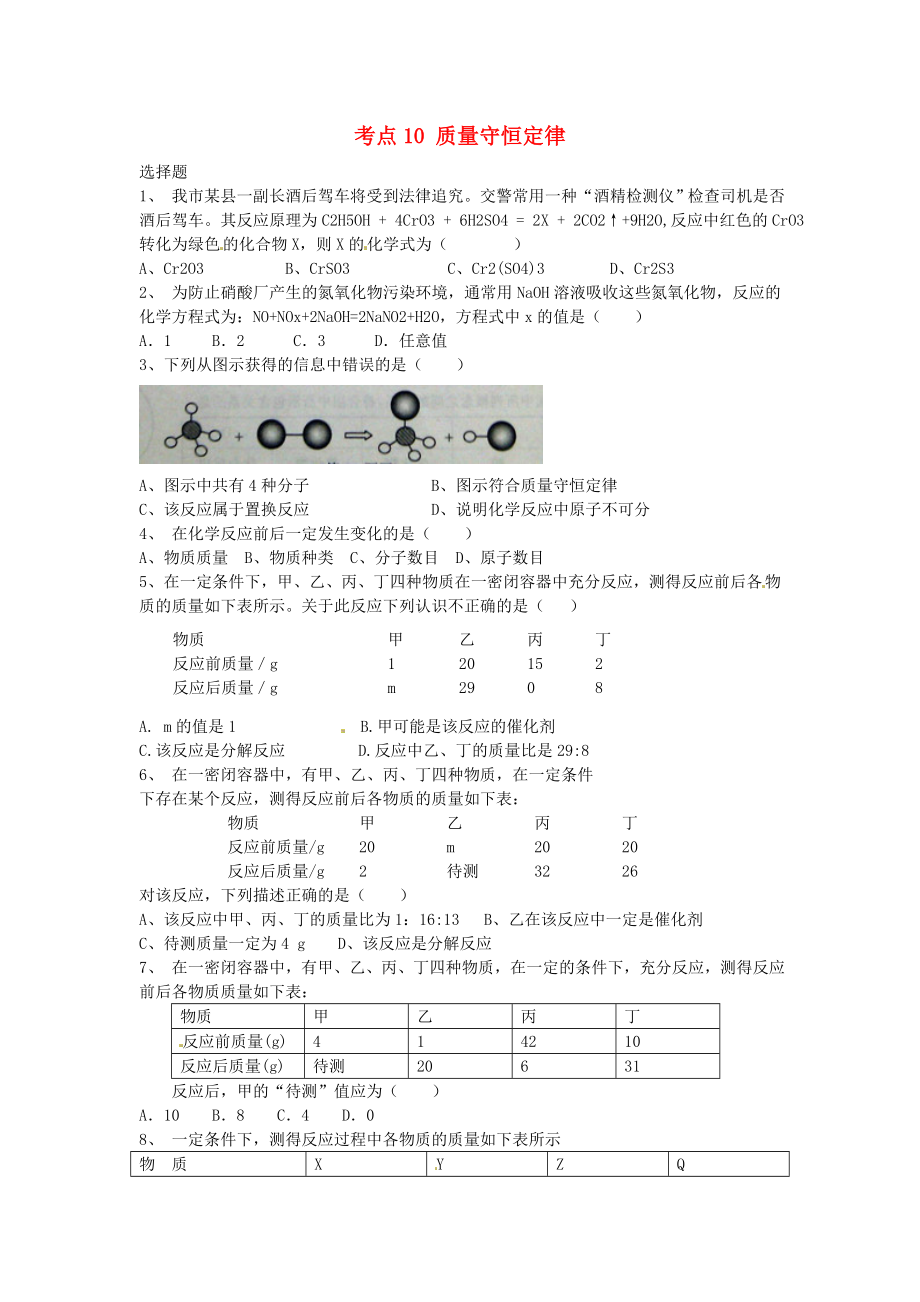
3、下列從圖示獲得的信息中錯(cuò)誤的是( )
A���、圖示中共有4種分子 B��、圖示符合質(zhì)量守恒定律
C����、該反應(yīng)屬于置換反應(yīng) D���、說(shuō)明化學(xué)反應(yīng)中原子不可分
4����、 在化學(xué)反應(yīng)前后一定發(fā)生變化的是( )
A、物質(zhì)質(zhì)量 B����、物質(zhì)種類(lèi) C、分子數(shù)目 D�����、原子數(shù)目
5���、 在一定條件下,甲��、乙����、丙、丁四種物質(zhì)在一密閉容器中充分反應(yīng)��,測(cè)得反應(yīng)前后各物質(zhì)的質(zhì)量如下表所示�����。關(guān)于此反應(yīng)下列認(rèn)識(shí)不正確的是( )
物質(zhì)
甲
乙
丙
丁
反應(yīng)前質(zhì)量/g
1
20
15
2
反應(yīng)后
3、質(zhì)量/g
m
29
0
8
A. m的值是1 B.甲可能是該反應(yīng)的催化劑
C.該反應(yīng)是分解反應(yīng) D.反應(yīng)中乙���、丁的質(zhì)量比是29:8
6����、 在一密閉容器中�����,有甲��、乙���、丙����、丁四種物質(zhì)���,在一定條件
下存在某個(gè)反應(yīng)�,測(cè)得反應(yīng)前后各物質(zhì)的質(zhì)量如下表:
物質(zhì)
甲
乙
丙
丁
反應(yīng)前質(zhì)量/g
20
m
20
20
反應(yīng)后質(zhì)量/g
2
待測(cè)
32
26
對(duì)該反應(yīng),下列描述正確的是( )
A�����、該反應(yīng)中甲�、丙、丁的質(zhì)量比為1:16:13 B����、乙在該反應(yīng)中一定是催化劑
C、待測(cè)質(zhì)量
4����、一定為4 g D、該反應(yīng)是分解反應(yīng)
7����、 在一密閉容器中,有甲����、乙���、丙��、丁四種物質(zhì)����,在一定的條件下,充分反應(yīng)���,測(cè)得反應(yīng)前后各物質(zhì)質(zhì)量如下表:
物質(zhì)
甲
乙
丙
丁
反應(yīng)前質(zhì)量(g)
4
1
42
10
反應(yīng)后質(zhì)量(g)
待測(cè)
20
6
31
反應(yīng)后��,甲的“待測(cè)”值應(yīng)為( )
A.10 B.8 C.4 D.0
8��、 一定條件下�,測(cè)得反應(yīng)過(guò)程中各物質(zhì)的質(zhì)量如下表所示
物 質(zhì)
X
Y
Z
Q
第一次測(cè)得的質(zhì)量/g
68
16
4.4
3.6
第二次測(cè)得的質(zhì)量/g
4
未測(cè)
48.4
39.6
5��、
下列判斷錯(cuò)誤的是( )
A該反應(yīng)一定是中和反應(yīng) B若X為氧氣����,則Y一定發(fā)生氧化反應(yīng)
C.第二次測(cè)量時(shí),Y已完全參加反應(yīng) D該反應(yīng)中z與Q質(zhì)量變化之比為11:9
9���、 質(zhì)量守恒定律是幫助我們認(rèn)識(shí)化學(xué)反應(yīng)實(shí)質(zhì)的重要理論����。在化學(xué)反應(yīng)aA+bB = cC+dD中�,下列說(shuō)法正確的是( )
A. 化學(xué)計(jì)量數(shù)a與b之和一定等于c與d之和
B. 若取xg A和xg B反應(yīng),生成C和D的質(zhì)量總和不一定是2xg
C. 反應(yīng)物A和B的質(zhì)量比一定等于生成物C和D的質(zhì)量比
D. 若A和C都是鹽,則該反應(yīng)一定是復(fù)分解反應(yīng)
10�、 在一密閉容器中,有甲�����、乙�、丙、丁四
6���、種物質(zhì)���,一定條件下充分反應(yīng),測(cè)得反應(yīng)前后各物質(zhì)的質(zhì)量如下表:
物質(zhì)
甲
乙
丙
丁
反應(yīng)前的質(zhì)量(g)
54
17
20
0
反應(yīng)后的質(zhì)量(g)
10
0
2
X
下列說(shuō)法正確的是( )
A.甲物質(zhì)全部反應(yīng)完 B.該反應(yīng)為分解反應(yīng)
C.參加反應(yīng)的丙物質(zhì)的質(zhì)量為20g D.x為79
11����、 下圖表示物質(zhì)A()與B()在一定條件下反應(yīng)生成C( )的微觀(guān)示意圖(和 表示兩種質(zhì)子數(shù)不同的原子)。下列說(shuō)法正確的是( )
A.該反應(yīng)在反應(yīng)前后其原子種類(lèi)沒(méi)有發(fā)生變化��,但原子數(shù)目減少
B .A
7��、�����、B��、C三種物質(zhì)在分類(lèi)上均屬于化合物
C.該反應(yīng)的化學(xué)方程式中���,A�、B�、C 的化學(xué)計(jì)量數(shù)之比為2:l:2 D.該反應(yīng)屬于復(fù)分解反應(yīng)
12、 根據(jù)化學(xué)方程式A+NaOH== B+H2O推斷����,B,A的相對(duì)分子質(zhì)量相差( )
A. 12 B. 18 C.22 D.40
13、 W��、X����、Y、Z四種物質(zhì)在一定條件下充分反應(yīng)后�,測(cè)得反應(yīng)前后各物質(zhì)的質(zhì)量如下:
物質(zhì)
W
X
Y
Z
反應(yīng)前質(zhì)量g
2
22
34
0
反應(yīng)后質(zhì)量g
2
40
待測(cè)
16
下列說(shuō)法錯(cuò)誤的是( )
A.W在反應(yīng)中可能是催化劑 B.該反應(yīng)中生成X的質(zhì)量為40g
C.該反應(yīng)屬于分解反應(yīng) D.該反應(yīng)中Y全部參加反應(yīng)
14、 在托盤(pán)天平兩邊各放一只等質(zhì)量的燒杯�����,在兩只燒杯里分別加入50g溶質(zhì)質(zhì)量分?jǐn)?shù)為7.3%的稀鹽酸���,將天平調(diào)節(jié)至平衡�;然后向左右兩燒杯中分別加入一定質(zhì)量的下列各組物質(zhì),充分反應(yīng)后���,天平發(fā)生偏轉(zhuǎn)的是( )
A.1.8g鋁粉和1.8g 鐵粉 B.4.2g碳酸鎂和2g硝酸銀
C.5.6g鐵粉和5.6g 鋅粉 D.10g碳酸鈣和5.6g氧化鈣
 天津市太平村中學(xué)2020年中考化學(xué)考點(diǎn)訓(xùn)練 質(zhì)量守恒定律(無(wú)答案)
天津市太平村中學(xué)2020年中考化學(xué)考點(diǎn)訓(xùn)練 質(zhì)量守恒定律(無(wú)答案)