《2019年九年級(jí)化學(xué)上冊(cè) 第五單元《化學(xué)方程式》課題3 利用化學(xué)方程式的簡(jiǎn)單計(jì)算課件 新人教版.ppt》由會(huì)員分享��,可在線閱讀����,更多相關(guān)《2019年九年級(jí)化學(xué)上冊(cè) 第五單元《化學(xué)方程式》課題3 利用化學(xué)方程式的簡(jiǎn)單計(jì)算課件 新人教版.ppt(13頁(yè)珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索。
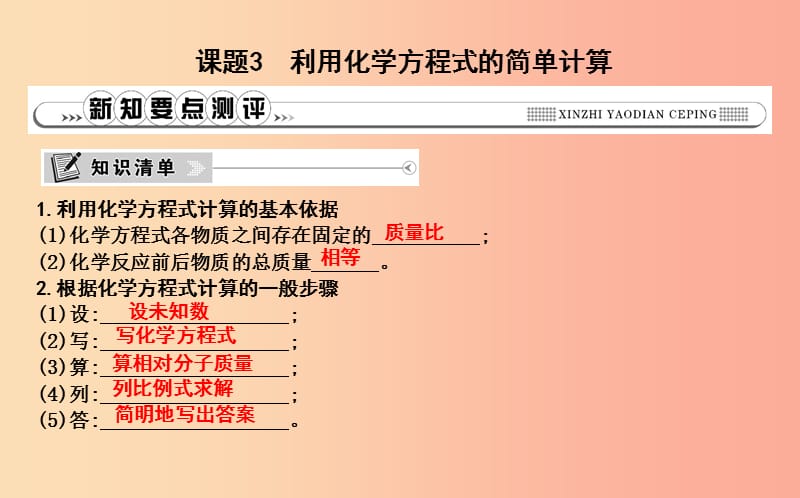
1�、課題3利用化學(xué)方程式的簡(jiǎn)單計(jì)算,1.利用化學(xué)方程式計(jì)算的基本依據(jù)(1)化學(xué)方程式各物質(zhì)之間存在固定的;(2)化學(xué)反應(yīng)前后物質(zhì)的總質(zhì)量。2.根據(jù)化學(xué)方程式計(jì)算的一般步驟(1)設(shè):;(2)寫:;(3)算:;(4)列:;(5)答:��。,質(zhì)量比,相等,設(shè)未知數(shù),寫化學(xué)方程式,算相對(duì)分子質(zhì)量,列比例式求解,簡(jiǎn)明地寫出答案,根據(jù)化學(xué)方程式計(jì)算的依據(jù),1.根據(jù)化學(xué)方程式計(jì)算是由于()A.化學(xué)方程式表示了一種化學(xué)反應(yīng)過程B.化學(xué)方程式表示了參加反應(yīng)的物質(zhì)是什么,反應(yīng)后生成的物質(zhì)又是什么C.化學(xué)方程式表示反應(yīng)前后反應(yīng)物和生成物的質(zhì)量關(guān)系D.在化學(xué)方程式中,各反應(yīng)物的質(zhì)量比等于各生成物的質(zhì)量比,C,根據(jù)化學(xué)方程式的
2���、計(jì)算需要注意的問題:(1)化學(xué)方程式一定要正確�。(2)相關(guān)物質(zhì)的數(shù)據(jù)要寫在對(duì)應(yīng)物質(zhì)的正下方�����。(3)計(jì)算中所用的質(zhì)量必須是實(shí)際參加反應(yīng)的物質(zhì)的質(zhì)量����。(4)計(jì)算過程中各物理量單位必須對(duì)應(yīng)統(tǒng)一,單位要代入計(jì)算過程。(5)體積要換算成質(zhì)量進(jìn)行計(jì)算��。(6)各代入量均指純凈物的質(zhì)量�����。若物質(zhì)不純,必須換算成純凈物的質(zhì)量才能代入化學(xué)方程式進(jìn)行計(jì)算。,,,根據(jù)化學(xué)方程式的簡(jiǎn)單計(jì)算,,,D,B,4.(2017杭州)在海底和凍土層存在著儲(chǔ)量巨大的“天然氣水合物”,具有良好的開發(fā)和應(yīng)用前景�。有科學(xué)家開采得到一種天然氣水合物樣品,取95.6g樣品放置在一密閉容器內(nèi),該樣品迅速轉(zhuǎn)化為甲烷氣體(CH4)和水,將甲烷氣體分離
3、并完全燃燒,得到35.2g二氧化碳�。求該天然氣水合物樣品中甲烷的質(zhì)量分?jǐn)?shù)。(結(jié)果精確到0.1%),,,,,根據(jù)化學(xué)方程式計(jì)算的步驟可概括為“一設(shè)���、二寫、三列���、四解��、五答”�����。一設(shè):設(shè)未知量�����。二寫:寫化學(xué)方程式�。三列:列出相關(guān)數(shù)據(jù)(化學(xué)計(jì)量數(shù)��、相對(duì)分子質(zhì)量)。四解:列出比例式,求解�。五答:簡(jiǎn)明地寫出答案。,,,B,C,A,D,5.某碳酸鈣和氧化鈣組成的混合物中鈣元素的質(zhì)量分?jǐn)?shù)為60%,將50g該混合物高溫煅燒至固體質(zhì)量不再改變,則生成二氧化碳的質(zhì)量是()A.6gB.8gC.13.2gD.20g6.(2017孝感)碳酸鋅與碳酸鈣具有相似的化學(xué)性質(zhì)?,F(xiàn)將12.5g碳酸鋅固體高溫煅燒一段時(shí)間,冷卻后,向
4、剩余固體中加入足量稀硫酸���。下列結(jié)論正確的個(gè)數(shù)是()①共生成16.1g硫酸鋅②煅燒越充分則消耗的硫酸越少③煅燒后固體中氧元素的質(zhì)量分?jǐn)?shù)減?、茏罱K生成二氧化碳的總質(zhì)量與煅燒時(shí)間的長(zhǎng)短有關(guān)A.1個(gè)B.2個(gè)C.3個(gè)D.4個(gè),B,B,,7.(2017山西)在一次實(shí)驗(yàn)課上,同學(xué)們用加熱氯酸鉀和二氧化錳混合物的方法制取氧氣��。他們?nèi)×?4.5g的混合物,其中二氧化錳的質(zhì)量分?jǐn)?shù)為20%,加熱到完全分解��。通過計(jì)算,得出他們制得氧氣的質(zhì)量是多少?,,8.(核心素養(yǎng)題)鎂銅合金常用作飛機(jī)天線等導(dǎo)電材料,現(xiàn)取某鎂銅合金10g放入燒杯中,加入足量稀硫酸充分反應(yīng)后,測(cè)得剩余固體的質(zhì)量是6.4g,請(qǐng)計(jì)算:(1)該鎂銅合金中鎂的質(zhì)量為g�����。,答案:(1)3.6,,(2)生成H2的質(zhì)量�����。,謝謝觀賞�!,
 2019年九年級(jí)化學(xué)上冊(cè) 第五單元《化學(xué)方程式》課題3 利用化學(xué)方程式的簡(jiǎn)單計(jì)算課件 新人教版.ppt
2019年九年級(jí)化學(xué)上冊(cè) 第五單元《化學(xué)方程式》課題3 利用化學(xué)方程式的簡(jiǎn)單計(jì)算課件 新人教版.ppt